|
|
Órgão Oficial de Divulgação Científica da
|
ISSN: 1679-1796
|
Indicações e Técnicas do Tratamento Laparoscópico do Câncer Gástrico
Indications and Techniques for Laparoscopic Surgical Treatment of Gastric Cancer
Cláudio Bresciani, Joaquim Gama-Rodrigues, Carlos Eduardo Jacob, Rodrigo Oliva Perez, Érica Helou Bresciani, Bárbara Helou Bresciani, Ulysses Ribeiro Júnior, Bruno Zilberstein
Trabalho realizado na Unidade de Cirurgia Laparoscópica da Divisão de Clínica Cirúrgica II do HCFMUSP (Disciplina de Cirurgia
do Aparelho Digestivo do Departamento de Gastroenterologia da FMUSP)
O objetivo do tratamento cirúrgico videolaparoscópico do câncer gástrico é oferecer cura a uma parcela dos
pacientes com a doença e também as vantagens da cirurgia minimamente invasiva. Ainda que a experiência com a
videocirurgia para a cura do câncer gástrico seja escassa e não haja adequado conhecimento sobre seus resultados, o objetivo dessa revisão
é conhecer as principais indicações e técnicas para o tratamento laparoscópico do câncer gástrico. As principais técnicas
videolaparoscópicas para o tratamento radical do câncer gástrico são a endogastrocirurgia, a ressecção laparoscópica em cunha e a gastrectomia distal
D1. O adenocarcinoma gástrico para o qual se admite a execução de tratamento radical por vídeo é aquele restrito à mucosa
como resultado da ocorrência excepcional de metástases linfonodais. Para o câncer gástrico com invasão de células neoplásicas na
submucosa ou mais profunda (avançado), a realização de linfadenectomia D2 pressupõe ainda a via de acesso convencional como a melhor
opção. A laparoscopia pode participar nesta fase como auxiliar no estadiamento das lesões evitando assim, em determinados casos,
a laparotomia desnecessária.
Palavras-chave: Câncer Gástrico; Procedimentos Cirúrgicos por Laparoscopia;
Gastrectomia; Procedimentos Cirúrgicos Endoscópicos
The laparoscopic therapeutic approach for surgical treatment of gastric cancer aims to offer cure for
selected patients in association to known benefits of the minimally invasive surgery. Although published experience
issuing this matter still remains limited, the objective of this review is to evaluate present indications and techniques. There are three
main technical options for laparoscopic treatment of gastric cancer: intra-gastric laparoscopic resection, wedge resection and
laparoscopic distal D1 gastrectomy. Laparoscopic surgical treatment for cure of gastric cancer may be offered for patients with
intramucosal malignancy as result of the exceptionally low rate of lymph node metastases. For early gastric cancer with invasion to the
submucosa or deeper (advanced), conventional resection associated to D2 lymphadenectomy remains best surgical option. For these
cases, however, staging laparoscopic may be a valuable preoperative tool in order to avoid unnecessary laparotomy for some patients.
Key words: Gastric Cancer; Laparoscopic Surgical Procedure; Laparoscopic Surgery;
Gastrectomy; Endoscopic Surgical Procedures
|
Bresciani C, Gama-Rodrigues J, Jacob CE, Perez RO, Bresciani ÉH, Bresciani BH, Ribeiro Júnior U, Zilberstein B. Indicações e Técnicas do Tratamento Laparoscópico do Câncer Gástrico. Rev bras videocir 2004;2(4):206-213. |
||
|
Recebido em 29/12/2004 |
|
Aceito em 30/12/2004 |
pós o estabelecimento da videocirurgia como importante arma do cirurgião
do aparelho digestivo foi natural que o tratamento do câncer gástrico (CG) passasse a
ser foco da atenção dos cirurgiões envolvido
no tratamento desta grave doença. O objetivo
é oferecer também a esta parcela de pacientes
as vantagens da cirurgia minimamente invasiva:
menor trauma, internação mais breve, rápido retorno
a atividades rotineiras e melhor resultado
cosmético (GAMA-RODRIGUES e cols., 1994).
Na cirurgia das vias biliares a fase evolutiva da doença da vesicular biliar ao ser operada
_ colecistite crônica calculosa com pouca
inflamação, colecistite aguda ou vesícula esclero-atrófica
_ interfere tão somente no grau de dificuldade
técnica enfrentada pelo cirurgião.
Entretanto, na cirurgia do câncer
gástrico a fase evolutiva da doença (Estádios de I a
IV) interfere não somente com a dificuldade técnica
do ato operatório, mas principalmente com a
perspectiva de cura oferecida a estes doentes, o que em
última instância define a sobrevivência destes pacientes.
É importante definir quais as vantagens serão auferidas pelos doentes com o uso
da videocirurgia conforme o avançamento (Estádio)
do CG no momento do tratamento.
As primeiras publicações sobre o
tratamento do CG por videocirurgia
KITANO e cols. (1994),
originadas
do Japão e de WATSON e cols.
(1995) do Ocidente.
As vantagens do método da videocirurgia aplicada ao tratamento do câncer gástrico
são: trauma cirúrgico menor, margem
cirúrgica suficiente, possibilidade de detalhado
exame histopatológico e possibilidade de
linfadenectomia perigástrica (OHGAMI e cols.,1998). Estes
autores têm grande experiência em cirurgia
laparoscópica para o CG e publicaram inúmeros trabalhos
com seus resultados (OHGAMI e cols., 1996, 1998, 1999, 2000). Entretanto, eles mesmos apontam
uma série de problemas a serem resolvidos no
tratamento laparoscópico do CG: diagnóstico preciso
pré-operatório da profundidade da invasão do
tumor na parede gástrica, possibilidade de
reoperação caso haja invasão da submucosa gástrica,
linfática ou venosa no exame histopatológico
final, possibilidade de estenose pós-operatória nas
lesões localizadas junto à cárdia e possibilidade
de tumores gástricos múltiplos (OHGAMI e
cols., 1998). Deve-se observar, entretanto, que
estes autores sempre publicam tratamento menos invasivo para o câncer gástrico somente na
fase precoce.
A posição de tradicionais grupos
japoneses quanto à abordagem do CG foi bem resumida
no artigo publicado em 1996 por MARUYAMA e cols. do tradicional
National Cancer Center de Tóquio, uma das maiores fontes irradiadoras da
normatização japonesa para o tratamento cirúrgico do CG.
Neste estudo Maruyama, Sasako, Ionoshita, Sano e
Katai revêm a cirurgia do CG e observam que:
· os resultados são melhores no Japão que
no Ocidente, mesmo após o ajuste por estádios,
· que os procedimentos cirúrgicos realizados
lá são mais agressivos e mais meticulosos que
os realizados em outros países,
· e em particular, destacam que a
dissecção linfonodal D2 é procedimento padrão na
maioria dos serviços e segue a racionalização
orientada por computador proposta há vários anos
por Maruyama.
A gastrectomia com margem macroscópica adequada e acompanhada de linfadenectomia
pelo menos D2 é o tratamento padrão para
o adenocarcinoma gástrico. E tem sido utilizada
no Serviço de Cirurgia do Estômago, Duodeno
e Intestino Delgado da Disciplina de Cirurgia do Aparelho Digestivo da Faculdade de Medicina
da Universidade de São Paulo (Prof.
Gama-Rodrigues) há pelo menos 30 anos obtendo-se resultados
de sobrevivência de cinco anos por
estádios semelhantes aos obtidos pelos melhores
serviços japoneses (MATSUDA, 1988). Neste estudo
a sobrevivência de cinco anos para o estádio I foi
de 80%, 72,3% no estádio II, 47,8% no estádio III
e nula no estádio IV.
Outro ponto de fundamental importância em relação a videocirurgia é a possibilidade
desta modalidade de tratamento operatório determinar
a implantação de células tumorais nas punções
dos trocartes e mesmo em outras áreas da
cavidade abdominal. (TAGARONA e cols., 1998;
LEFOR, 2000). Vários aspectos são intervenientes na
questão da disseminação neoplásica, e devem
ser esclarecidos. Destacam-se: a laparoscopia pela presença do pneumoperitônio promove a
mobilização de células, estas podem se aderir ao local da
punção dos trocartes, sendo possível identificarem-se
células neoplásicas nos instrumentos, nos trocartes e no
gás exalado pelos últimos; outro aspecto diz respeito
à interferência do pneumoperitônio sobre
o crescimento tumoral e sobre a
imunocompetência do paciente. Por estas razões pode a
cirurgia videolaparoscópica não ser método adequado
para o tratamento de doenças neoplásicas,
especialmente se houver a possibilidade da superfície serosa
do órgão estar acometida pela neoplasia.
LEFOR (2000) propõe que somente se empregue a videocirurgia em doenças
neoplásicas como diagnóstico e estadiamento e reservar
a ressecção terapêutica para estudos controlados
por centros especializados, devendo ser as
investigações prospectivas e aleatorizadas.
O princípio do tratamento do
câncer orientado pelo estádio da moléstia no momento
do diagnóstico é uma norma geral na oncologia e
deve ser estendida ao campo do tratamento cirúrgico
do CG. Muito embora a gastrectomia total ou
subtotal realizadas levando-se em consideração a sede
do tumor no estômago e acompanhada de linfadenectomia D2, seja hoje de grande aceitação,
é desejável que a escolha do procedimento
cirúrgico seja adotado para cada caso e adaptado ao
estádio do paciente (HERMANEK, 1996). Além do
que, apesar dos excelentes resultados obtidos no Japão
e também nos países do Ocidente com o
tratamento do CGP através de gastrectomia D2,
considerando-se a baixa mortalidade e a sobrevivência a
longo prazo, a verdade é que a morbidade e as
seqüelas da ressecção gástrica são bastante
significativas (PATHIRANA e POSTON, 2001).
O câncer gástrico apresenta-se nas
seguintes fases evolutivas: precoce, intermediário,
avançado e disseminado. Exceto a última fase as outras
três são passíveis de tratamento radical e, portanto,
a cura pode ser obtida. É claro que se obtém
maior índice de cura nos casos precoces, depois
nos intermediários e por último nos
avançados (BRESCIANI e cols., 2000).
É notório que há um leque de
opções terapêuticas para o CG e que dependem do
estádio da doença e da possibilidade técnica da
cirurgia laparoscópica.
As opções de tratamento para o CG
desde o menos invasivo até o tratamento padrão -
a gastrectomia subtotal ou total D2 - são
os seguintes:
1. mucosectomia
2. fulguração por endoscopia
3. ressecção gástrica em cunha
4. gastrectomia D0
5. gastrectomia D1 e
6. gastrectomia D2.
A fulguração de lesões gástricas
somente deve ser usada em situações de exceção e,
portanto, não esta recomendada por dificultar a avaliação
da qualidade do tratamento e por não permitir a
análise histológica do tumor gástrico. A gastrectomia
D2 não é procedimento realizável por videocirurgia
com o atual desenvolvimento desta modalidade
cirúrgica, e, portanto, não esta incluída dentro
das possibilidades terapêuticas que empregam
a laparoscopia.
Neste capítulo serão analisadas as
indicações do tratamento laparoscópico e sua
técnica conforme a fase do CG a ser tratado:
precoce, avançado (incluindo os tumores intermediários)
e disseminado.
Câncer Gástrico Precoce
A análise do câncer gástrico precoce
(CGP) quando comparado com o CG avançado mostra
uma situação totalmente diversa tanto em relação
à disseminação linfonodal quanto à sobrevivência.
É pouco comum o acometimento linfonodal nesta fase da doença e a sobrevivência
observada aos cinco anos de seguimento para os
doentes submetidos a tratamento cirúrgico radical
com ressecção linfonodal D2 aproxima-se de 100%.
Alguns estudos demonstram que o comprometimento linfonodal no CGP
correlaciona-se principalmente com as seguintes
variáveis: tamanho do tumor, intensidade e profundidade
da invasão na submucosa, aspecto macroscópico,
tipo histológico e intensidade da invasão vascular
(HIKI e cols., 1992; ICHIKURA e cols., 1995). REPSE
e cols. (2001) em recente análise
multivariada encontrou que a penetração do tumor na
parede gástrica, o tipo histológico segundo a
classificação de Lauren e parcialmente o tamanho do tumor
são os principais fatores relacionados à presença ou
não de acometimento linfonodal.
As metástases linfonodais apenas
excepcionalmente ocorrem nos tumores precoces com invasão limitada à mucosa gástrica, do
tipo macroscópico I (protuso) ou IIa
(superficialmente elevado) ou IIb (plano) ou IIc (deprimido)
sem ulceração ou cicatriz de úlcera, do tipo
histológico intestinal e que não sejam maiores que 2 cm.
Estes tumores muito excepcionalmente apresentam acometimento linfonodal. Portanto neste
grupo muito específico de CGP é possível tratamento
mais limitado e que ainda seja radical. A
linfadenectomia não é necessária e podem-se utilizar as
seguintes modalidades terapêuticas: ressecção
endoscópica, ressecção em cunha trans-laparoscópica,
ressecção por endogastrocirurgia, gastrectomia Dl por
vídeo-cirurgia ou ainda por laparotomia. Um certo
número de pacientes com CGP por terem risco de
apresentar metástase apenas para linfonodos do nível 1
(N1), poderiam ser tratados por gastrectomia D1
por laparotomia ou até por vídeo-cirurgia
(GAMA-RODRIGUES e cols., 1986; NAGAI e cols.,
1995). A figura 1 demonstra lesão elevada e limitada
à mucosa pela ecoendoscopia.
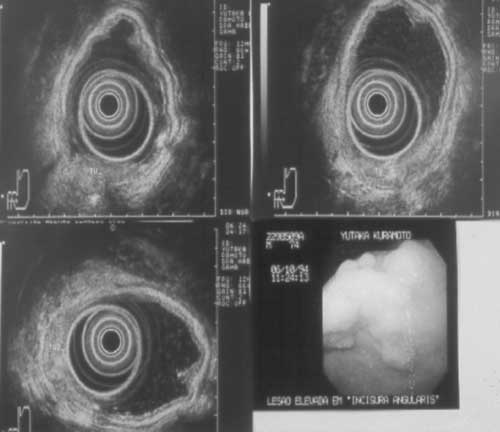 |
| Figura 1 - Lesão elevada e limitada à mucosa conforme determinado pela ecoendoscopia. |
Para a realização técnica da
ressecção em cunha
laparoscópica (Figura 2), procede-se após
a realização do pneumoperitônio, à
minuciosa inspeção da cavidade. Procede-se então
à endoscopia per-oral para localização precisa da
lesão no estômago. Com o auxílio da endoscopia,
procede-se à demarcação do tumor na face serosa
do estômago.Antes da ressecção, o
endoscopista procede à aspiração do ar insuflado no interior
da câmara gástrica. Para a realização da
operação, procede-se à tração da parede gástrica
formando uma tenda e à secção gástrica com
endogrampeador. A peça é retirada da cavidade em saco plástico
de proteção e procede-se imediatamente à
avaliação macroscópica e microscópica das margens
cirúrgicas obtidas.
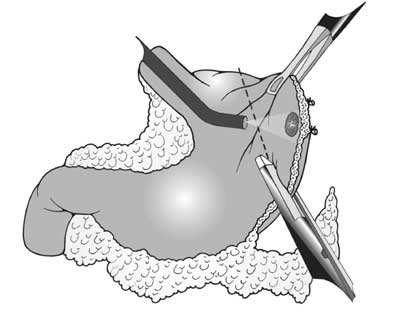 |
| Figura 2 - Técnica da ressecção em cunha laparoscópica |
Para a realização da técnica de
endogastrocirurgia (Figura 3), procede-se à insuflação
do estômago através da sonda gástrica e a acesso
aberto à cavidade abdominal e ao estômago. Após,
é realizado o posicionamento intragástrico de
três trocartes com balão, que ancoram a parede
gástrica na parede abdominal e à instalação do
pneumogastro. Após o posicionamento das pinças de
trabalho para a ressecção intragástrica, esta é realizada
sob visão direta e com auxilio do
eletrocautério. Finalmente, procede-se à retirada da peça em
saco plástico de proteção e avaliação das
margens cirúrgicas obtidas.
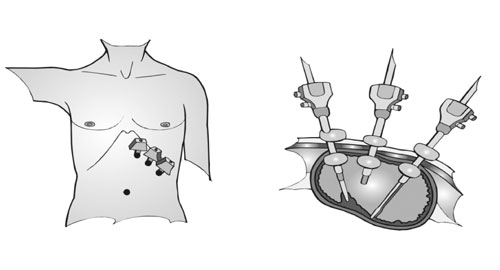 |
| Figura 3 - Técnica da endogastrocirurgia. |
Para a realização da gastrectomia distal
D1 (Figura 4), após a pneumoperitônio, a dissecção
do grande omento além da arcada gástrica permitirá
a retirada dos linfonodos N1 (perigástricos).
O pequeno omento é dissecado próximo ao fígado
o que permitirá a retirada dos linfonodos N1.
O duodeno é então seccionado com
endogrampeador, assim como o estômago. Após a retirada da peça
em saco plástico de proteção (eventualmente
é necessária à ampliação da entrada de um
dos trocartes), procede-se à avaliação do aspecto
da lesão e das margens cirúrgicas. A reconstrução
é realizada através de anastomose gastro-jejunal
em Y de Roux com endogrampeador. Procede-se
então à sutura dos orifícios de entrada dos ramos
do grampeador e à anastomose jejuno-jenunal
com endogrampeador.
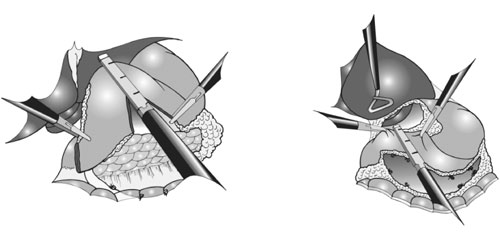 |
| Figura 4 - Técnica da gastrectomia distal D1 |
Muito embora existam inúmeras propostas de cirurgia mais limitada para o tratamento
radical do câncer gástrico precoce é impressão dos
autores que a opinião de YOKOTA e cols. (2003) é
acertada frente a pouca experiência com estes
procedimentos, isto é, a cirurgia limitada deve
ser considerada experimental e somente realizada em protocolos
de pesquisa rigorosamente controlados. Para tais
estudos a existência dos seguintes recursos é indispensável:
1. Endoscopista treinado para o diagnóstico
do câncer gástrico precoce
2. Endoscopista habilitado a realizar ecoendoscopia
3. Respeito aos critérios de indicação
4. Instrumental específico
5. Equipe cirúrgica habilitada ao tratamento
do câncer gástrico precoce por cirurgia
mini-invasiva gástrica
6. Equipe cirúrgica habilitada ao
tratamento convencional do câncer gástrico precoce
7. Patologista habilitado ao diagnóstico do
câncer gástrico
8. Cientificar o paciente da possibilidade da reintervenção cirúrgica
9. Possibilidade de realizar detalhado
seguimento clínico e endoscópico
CÂncer GÁstrico AvanÇado
Quando se analisa o câncer
avançado passível de ressecção curativa, recomenda-se
a atuação cirúrgica agressiva, ou seja, a
gastrectomia total ou subtotal, na dependência da localização
do tumor no estômago, com margem macroscópica
livre de tumor de pelo menos 5 cm e mais alargada
ainda caso o tipo histológico seja o indiferenciado
de Nakamura além de linfadenectomia extensa que
seja no mínimo D2. Tem-se experimentado uma
maior extensão da linfadenectomia para D3 ou D4 com
o objetivo de melhorar os índices de sobrevivência,
o que ainda não se logrou confirmar.
Nesta fase da doença a freqüência
de acometimento linfonodal é alta e é, portanto,
para estes doentes que deve o cirurgião estar
preparado para realizar a adequada linfadenectomia e nela
se esmerar durante o ato operatório, uma vez
que outros métodos de tratamento (quimio e radioterapia) não conseguem obter a cura e
tem somente ação complementar à cirurgia (Bresciani
e cols., 2000).
Portanto, não se recomenda à tentativa
de realizar a gastrectomia com linfadenectomia D2
para os tumores avançados através da videocirurgia.
Esta posição adotada na Disciplina de Cirurgia
do Aparelho Digestivo da Faculdade de Medicina da Universidade de São Paulo é idêntica ao
resultado do Consenso Brasileiro em Linfadenectomia
no Tratamento do Câncer Gástrico, realizado em
2001 por ocasião do Congresso Brasileiro de Cirurgia
do Colégio Brasileiro de Cirurgiões (Savassi-Rocha
e cols., 2001).
CÂncer GÁstrico Disseminado
No extremo do espectro de evolução
do adenocarcinoma gástrico encontra-se a
doença disseminada ou metastática. Neste caso,
a possibilidade de cura já desapareceu e o
tratamento cirúrgico visa tão somente oferecer maior
conforto e sobrevivência digna, sendo, portanto,
quando indicado, meramente paliativo. Assim
podem-se realizar: derivações externas (gastrostomia
e jejunostomia), derivações internas
(gastroenteroanastomose, enteroenteroanastomose), ressecção
em cunha ou gastrectomia. Por laparoscopia pode-se também realizar uma antiga modalidade
operatória descrita por DEVINE em 1925 e adaptada
a videocirurgia: a exclusão antral de tumor
obstrutivo com gastroenteroanastomose, revivida
por AMMORI e BOREHAM (2002).
Todos estes procedimentos podem ser realizados por meio do acesso
videolaparoscópico. Os riscos de disseminação peritonial ou
implante nos pontos de punção tornam-se pouco
relevantes frente à fase disseminada da doença neoplásica.
ConclusÕes
1. O tratamento do câncer gástrico avançado,
que é o mais freqüente em nosso meio, é cirúrgico
e permanece o padrão recomendado pela
escola japonesa: gastrectomia convencional com margem de segurança adequada e
linfadenectomia pelo menos D2. A laparoscopia pode participar nesta fase como auxiliar
no estadiamento das lesões evitando assim,
em determinados casos, a laparotomia desnecessária, mas não se recomenda a tentativa
de realizar a gastrectomia subtotal ou total D2
por videocirurgia.
2. Alguns tipos muito especiais de câncer
gástrico precoce podem ser tratados por
cirurgia minimamente invasiva, mas somente em protocolos de pesquisa controlados. A
técnica cirúrgica escolhida: gastrectomia assistida
(D1), ressecção em cunha ou a
endogastrocirurgia dependerão fundamentalmente da
localização do tumor.
3. Como terapêutica paliativa a laparoscopia
pode ser utilizada com liberdade.
4. Em que pese a menor agressão promovida
pela videocirurgia quando comparada com a intervenção convencional, esta última
deve mais econômica que laparoscópica.
5. A maioria das casuísticas não é numerosa
e carecem de seguimento adequado para avaliação dos resultados das intervenções
mini-invasivas.
Referências Bibliográficas
1. Ammori BJ, Boreham B. Laparoscopic Devine
exclusion gastrenterostomy for the palliation of unresectable
and obstructing gastric carcinoma. Surg Laparosc
Endos Percutan Tech 2002; 12 (5):353-5.
2. Bresciani C, Gama-Rodrigues J, Jacob C. E, Verotti
MG, Inoue M. Tratamento cirúrgico do câncer
gástrico precoce do estômago - In: Habr-Gama A,
Gama-Rodrigues J, Cecconello I, Zilberstein B, Machado MCC,
Saad WA, et al, eds. Atualização em Cirurgia do
Aparelho Digestivo e em Coloproctologia, São Paulo: Frontis
Editorial. 2000. p. 71-82.
3. Bresciani CJC, Gama-Rodrigues JJ, Strassmann
V, Waitzberg DL, Matsuda M, Pinotti HW. Long term
(five year) survival following radical surgical treatment
plus adjuvant chemotherapy (FAM) in advanced gastric
cancer. A controlled study. Rev Hosp Clin Fac Med S
Paulo 2000: 5:129-36.
4. Gama-Rodrigues J, Bresciani C, Waitzberg DL,
Matsuda M, Iryia K, Pinotti HW. Management of gastric
carcinoma. Extent of gastric resection and lymphadenectomy.
Currents trends and results. Arq Bras Cir Dig 1986;1:84-9.
5. Gama-Rodrigues J, Bresciani C, Sousa Jr AHS,
Arab-Fadul R, Habr-Gama A. A video-laparoscopia
nas afecções cirúrgicas do aparelho digestivo. In: Raia
AA, Zerbini EJ, eds. Clínica Cirúrgica Alípio Corrêa Netto.
4ª edição. São Paulo: Sarvier. 1994. p. 979-90.
6. Hermanek P. Differential surgical procedure in
curative therapy of stomach carcinoma. Leber Magen Darm
1996; 26: 64.
7. Hiki Y, Shimao H, Mieno H, Sakakibara Y. Laser
therapy for early upper gastrointestinal carcinoma. Surg
Clin North Am 1992; 72: 571-80.
8. Ichikura T, Uefuji K, Tomimatsu S, Okusa Y, Yahara
T, Tamakuma S. Surgical strategy for patients with
gastric carcinoma with submucosal invasion. A
multivariate analysis. Cancer 1995; 76:935-40.
9. Kitano S, Isso Y, Moriyama M, Sugimachi K.
Laparoscopy-assisted Billroth I gastrectomy. Surg Laparosc Endosc
1994; 4:146-8.
10. Lefor AT. The role of laparoscopy in the treatment
of intra-abdominal malignancies. Cancer J Sci Am 2000;
6 (Suppl 2): S159-68.
11. Maruyama K, Sasako M, Kinoshita T, Sano T, Katai
H. Surgical treatment for gastric cancer: the Japanese
approach. Semin Oncol 1996; 23:360-8.
12. Matsuda M. Inter-relação de aspectos histopatológicos
e o prognóstico no câncer gástrico após tratamento
cirúrgico radical [tese _ doutorado]. São Paulo: Faculdade
de Medicina, Universidade de São Paulo; 1998.
13. Nagai Y, Tanimura H, Takifuji K, Kashiwagi H,
Yamoto H, Nakatani Y. Laparoscope-assisted Billroth
I gastrectomy. Surg Laparosc Endosc 1995; 5: 281-7.
14. Ohgami M, Otani Y, Furukawa T, Kubota T, Kumai
K, Kitajima M. Curative laparoscopic surgery for early
gastric cancer: eight years experience. Nippon Geka
Gakkai Zasshi 2000; 101: 539-45. (article in Japanese)
15. Ohgami M, Otani Y, Kumai K, Kubota T, Fujita K,
Igarashi N, et al. Laparoscopic surgery for early gastric
cancer—its advantages and pitfalls. Gan To Kagaku Ryoho
1998; 25:484-92. (article in Japanese)
16. Ohgami M, Otani Y, Kumai K, Kubota T, Kim
YI, Kitajima M. Curative laparoscopic surgery for early
gastric cancer: five years experience. World J Surg
1999; 23:187-92.
17. Ohgami M, Otani Y, Kumai K, Kubota T, Kitajima M
. Laparoscopic surgery for early gastric cancer. Nippon
Geka Gakkai Zasshi 1996; 97:279-85. (article in Japanese)
18. Pathirana A, Poston GJ. Lessons from Japan -
endoscopic management of early gastric and oesophageal
cancer. Eur J Surg Oncol 2001; 27: 9-16.
19. Repse A, Kivam R, Krizman I, Repse S. Predictive
factors for regional lymph node involvement in early
gastric cancer patients. Proceedings of the
4th International Gastric Cancer Congress; 2001; New York; p.568.
20. Savassi-Rocha PR, Rodrigues MAG, Malheiros
CA, Bresciani C, Linhares ERM, Nectoux M, Possik
R, Kobayasi S. CBC Boletim Informativo (Edição
Especial), ano XXXII, 2001.
21. Targarona EM, Martinez J, Nadal A, Balague C,
Cardesa A, Pascual S, et al. Cancer dissemination
during laparoscopic surgery: tubes, gas, and cells. World J
Surg 1998; 22:55-60.
22. Watson DI, Devitt PG, Game PA, Laparoscopic
Billroth II gastrectomy for early gastric cancer. Br J Surg
1995; 82: 661-2.
23. Yokota T, Ishiyama S, Saito T, Teshima S, Shimotsuma
M, Yamauchik H. Treatment strategy of limited surgery
in the treatment guidelines for gastric cancer in Japan.
Lancet Oncol 2003; 4: 423-28.
ENDEREÇO PARA CORRESPONDÊNCIA
Cláudio Bresciani
Rua Jesuíno Arruda 122 ap. 141C
04532 - 080
São Paulo (SP)
